El peróxido de hidrogeno (H2O2), conocido también como agua oxidada fue producido en 1818 por el químico francés Louies Jacques Thénard, lo logró a través de la reacción de peróxido de bario y ácido nítrico. La fórmula correcta del peróxido de hidrógeno se describió finalmente a fines del siglo XIX (Abdollahi y Hosseini, 2014).
El peróxido de hidrógeno se caracteriza por tener en su composición hidrogeno y peróxido, es un compuesto generalmente líquido, incoloro e inestable que se descompone rápidamente en oxígeno y en agua con liberación de calor, lo cual no genera daño en el medio ambiente por eso es considerado como un desinfectante natural (Rao et al., 2013; McDonnell y Russell, 1999) aprobado por la FDA (Food and Drug Administration) y la EPA (United States Environmental Protection Agency).
El peróxido de hidrógeno es un fuerte oxidante (Pinto et al.,2006), esto se debe a su estructura química que posee electrones no apareados esto lo hace altamente reactivo, el cual le da la capacidad de dañar la estructura de microorganismos (bacterias, hongos y esporas) y agentes infecciosos (virus) compuestos por proteínas, lípidos y ácidos nucleicos (Abdollahi y Hosseini, 2014).
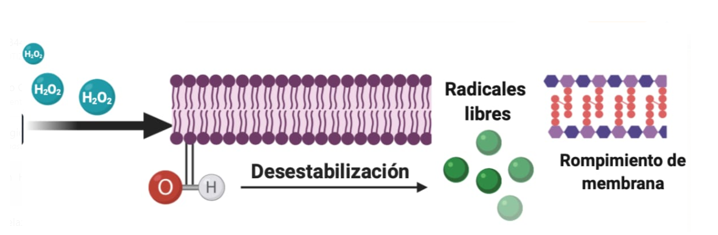
El peróxido de hidrogeno (H2O2) es de amplio uso como antiséptico, desinfectante y esterilizante. Es considerado biocida por que ha demostrado un amplio espectro en la actividad antimicrobiana, tiene baja toxicidad y se descompone el gua y oxígeno en el medio ambiente.
El peróxido de hidrógeno comercial se estabiliza para evitar o ralentizar su descomposición (Kampf,2018) ya que por sí sólo no es eficaz, por lo que no se aconseja utilizarlo como desinfectante único. Combinaciones con ácido peracético potencializan la acción desinfectante y el mecanismo de oxidación de ambos compuestos químicos, proporcionando mayor efectividad para inactivar, controlar y eliminar microorganismos (Amo et al., 2018; Aguilar et al., 2011).
Referencias
- Aguilar M. y Durán T. C. 2011.Química recreativa con agua oxigenada. Revista Eureka sobre Enseñanza y Divulgación de las Ciencias. EUREKA Cádiz, España. Vol. 8. pp. 446-453
- Amo H., Anraku D., Itarashiki T., Taniguchi T. y Hayashi, Nobuya. 2018. Sporicidal Activity of ‘Peracetic Acid-containing Hydrogen Peroxide Gas Sterilizer’. Iryou kikigaku (The Japanese journal of medical instrumentation).
- Joshi K., Mahendran R., Alagusundaram K., Norton T. y Tiwari B.K. 2013. Novel disinfectantsforfreshproduce.Trendsin FoodScience&Technology.34:54-61.
- Kampf, Günter. 2018. Hydrogen Peroxide
- McDonnell, G. and Russell, A. 1999. Antiseptics and disinfectants: activity, action and resistance. Clinical Microbiology Reviews, 12: 147-179.
- Pinto G., Castro A. C. M., Martínez U. J. 2006. Química al alcance de todos. Madrid. Pearson Educación. pp. 142-143.
- Rao, A. Mohan, H. & Iskra, Jernej. (2013). Hydrogen Peroxide.
- CFR21: https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/cfrsearch.cfm
- EPA: https://www.epa.gov/
